

초등학교 과학 시간에 과산화수소를 가지고 산소를 만드는 실험을 한 기억이 누구에게나 있을 것입니다. 이때 과산화산소와 반응하여 산소를 발생시키는 물질이 바로 ‘이산화망간’입니다. 이산화망간은 알카리 건전지를 포함한 다양한 1차 전지(충전이 되지 않는 전지)의 대표적인 양극 물질로 사용되고 있습니다.
망가니즈(Mn)라는 이름은 현재 그리스에 속해 있는 마그네시아 지방에서 발견된 두 종류의 검은색 광물을 지칭하는 말이었습니다. 18세기 중반, 스웨덴의 화학자 칼 셸레는 이산화 망가니즈를 포함한 광석에서 염소(Cl) 기체를 얻는 실험을 하던 중, 이 광물 안에 새로운 원소가 포함되어 있다는 사실을 알아냈습니다. 그러나 셸레는 그 원소를 분리해내지는 못했습니다. 이후 1774년, 요한 고틀리브 간은 이산화 망가니즈를 탄소와 반응시켜 산소를 제거한 뒤, 불순물이 섞인 형태의 망가니즈를 최초로 분리해냈습니다.
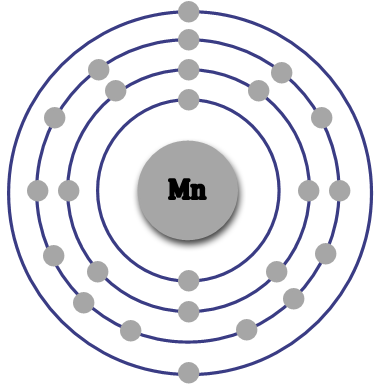
원자번호 25번의 망간(Mn)의 원소기호는 Mn입니다. 망간(Mn)은 지각에서 무게로 약 0.1% 정도 존재하는 물질로 12번째로 풍부한 원소입니다. 광물로는 이산화망간(Pyrolusite)이나 갈망가니즈석(Braunite)으로 존재하며 바닷물에는 10ppm 수준으로 들어있지만, 해저에는 5,000억톤으로 추정되는 망간(Mn) 단괴가 있다고 합니다. 전 세계 망가니즈(Mn) 매장량의 80%는 아프리카 지역에 있는 것으로 알려져 있으며. 이외에 우크라이나, 오스트레일리아, 인도, 중국, 가봉, 브라질 등에도 상당량이 매장되어 있습니다.


철강산업에서의 망간(Mn)은 합금원소로 사용되어 철강재의 강도를 높이는 역할 뿐만 아니라 철강제품의 제조에 있어서도 중요한 역할을 수행하고 있습니다. 우선 철강제품 제조 공정에서 황(S)과 결합하여 MnS를 만든 후 슬래그로 제거되어 철강제품에서 황을 제어하는 용도로 사용됩니다. 일반적으로 철강제품에서 황 성분이 높으면 황화철(FeS)이 생성되어 철강재가 잘 깨지는 취성(Brittleness, 脆性)이 나타나기 때문입니다. 또한 망간(Mn)은 산소와 결합하여 철강제품 내의 기포나 미세 구멍이 생기는 것을 막아 주기도 합니다. 망간(Mn) 함량이 40% 이상인 고품위 광석 기준으로 세계 매장량이 약 6억8천만톤 수준으로 추정되며, 연간 망간 생산량은 약 3,500만톤 수준인데 약 90%가 철강산업에서 소비되고 있습니다.

망가니즈(Mn)는 우수한 전자기적 특성을 띱니다. 그래서 자석을 만들 때도 소량의 망가니즈를 더해 자력을 강화합니다. 우리가 흔히 사용하는 AA 크기와 AAA 크기의 1.5V건전지에도 망가니즈가 첨가돼 있습니다. 전해액에 따라 망간 전지와 알칼리 전지를 통틀어 건전지라고 부르며, 1차 전지로서 일단 방전된 것은 다시 충전할 수가 없습니다.

| 발견자 | 요한 고틀리에브 간(Johan Gottlieb Gahn) | ||||
| 발견 연도 | 1774년 | ||||
| 어원 | 그리스에서 출토되는 '마그네시아(Magnesia)석' | ||||
| 특징 | 무르고, 전자기적 특성을 띤다. | ||||
| 사용 분야 | 망가니즈 합금, 자석, 건전지, 생체 기능 유지 등 | ||||
| 원자량 | 54.94 g/mol | ||||
| 밀도 | 7.47 g/cm3 | ||||
| 녹는점 | 1,246 °C | ||||
| 끓는점 | 2,061 °C | ||||
| 상온에서 상태 | 고체 | ||||
'지식data > 화학 DATA' 카테고리의 다른 글
| 인류 문명의 시작 원자번호 26번 철(Fe) (0) | 2022.02.02 |
|---|---|
| 인류 문명의 시작 원자번호 26번 철(Fe) (0) | 2022.02.02 |
| 원자번호 24번 녹슬지 않은 철 크로뮴,크롬(Cr) (0) | 2022.01.29 |
| 포드( Ford)가 사랑한 광물 원자번호 23번 바나듐(V) (0) | 2022.01.27 |
| 완벽에 가까운 원소 원자번호 22번 티타늄(Ti) (0) | 2022.01.25 |